Radioattivitŕ spontanea
In natura esistono diversi tipi di nuclei atomici che generalmente possono
essere suddivisi in due gruppi: i nuclei stabili e i nuclei instabili. Prima di tutto
dobbiamo rispondere ad una domanda fondamentale giŕ proposta a Rutherford
quando espone il suo modello atomico: "perché all’interno di quella
ristrettissima regione di spazio chiamata nucleo i protoni (che hanno
cariche dello stesso segno) non si respingono?" La risposta a questa domanda ci č
stata data dal famoso fisico italiano Enrico Fermi che scoprě l’esistenza
all’interno del nucleo di una forza aggregante(chiamata forza di Fermi o forza di
interazione forte) maggiore della forza di repulsione, per la quale i protoni, o meglio i
nucleoni non si dividono sparpagliandosi, ma rimangono vicini e compatti all’interno
del nucleo. Questa č una forza molto intensa ma agisce solamente su distanze estremamente
piccole, tanto da essere chiamata anche forza "a breve raggio".
A questo punto ci possiamo chiedere da che cosa dipende in definitiva la stabilitŕ di un
nucleo; ma, per rispondere, dobbiamo considerare alcuni punti.
Il nucleo č tanto piů stabile quanto piů elevata č la sua energia di legame
nucleare.
Un nucleo č stabile dal punto di vista energetico, cioč non emette spontaneamente
radiazioni, finché il numero dei protoni č circa uguale al numero dei neutroni: questo
si verifica quando 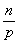 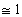 con n=numero neutroni e p=numero protoni. (grafico rapporto
n/p) con n=numero neutroni e p=numero protoni. (grafico rapporto
n/p)
Come ogni altro sistema fisico in equilibrio energetico instabile, anche il nucleo
degli elementi radioattivi tende spontaneamente ad uno stato di maggior stabilitŕ (a
energia minima) e lo realizza emettendo energia sottoforma di radiazioni di varia
natura. Stabilito che Z=numero atomico ad A=numero di massa di un atomo, questo
processo noto con il nome di decadimento radioattivo, avviene con modalitŕ diverse a
seconda dei casi: |
 |
|
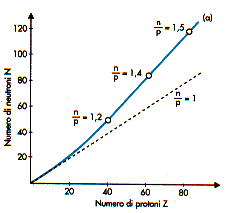
Rapporto neutroni/protoni nei nuclidi stabili. I nuclidii stabili
si dispongono in una fascia intorno alla linea (a) che, fino a Z=20coincide praticamente
con la retta n/p=1, poi se ne discosta al prevalere di n su p. Al di fuori della fascia si
trovano i nuclidi intabili (n/p molto elevato), che decadono spontaneamente a nuclidi
stabili (radioattivitŕ spontanea) |
Z>82 e A>200: si ha il decadimento a.
Negli elementi ad elevato numero atomico sono presenti sempre in maggior sovrannumero i
neutroni, per bilanciare le sempre piů intense forze di repulsione coulombiana dei
protoni. Il nucleo, in questo caso, decade emettendo un nucleo di elio (cioč due protoni
e due neutroni legati fra loro) chiamato appunto radiazione a.
Le radiazioni a sono di natura corpuscolare (ovvero sono delle
particelle che possiedono una determinata massa 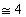 u.m.a.) e
rispetto alle altre sono le meno penetranti poiché possono essere fermate da una
finissima lamina metallica o circa 8cm d’aria. Sono comunque sia carcerogene che
mutagene. Viaggiano a circa 20000Km/s.
u.m.a.) e
rispetto alle altre sono le meno penetranti poiché possono essere fermate da una
finissima lamina metallica o circa 8cm d’aria. Sono comunque sia carcerogene che
mutagene. Viaggiano a circa 20000Km/s.
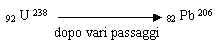
ovvero radiazioni per 4,5 miliardi di anni
- Con un rapporto
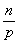 >1 (dove n č
il numero dei neutroni e p quello dei protoni): il nucleo contiene troppi neutroni
rispetto ai protoni; diventa piů stabile se uno dei suoi neutroni decade a protone dando
luogo al decadimento b. Ciň significa che il numero
di massa rimane costante, ma il numero atomico Z aumenta per ogni decadimento b di un’unitŕ, poiché ogni neutrone
emettendo un elettrone (i cosiddetti raggi b) e un neutrino
(una particella di massa molto piů piccola di quella dell’elettrone) si
"trasforma" in un protone. Le cosiddette radiazioni b
sono sempre di natura corpuscolare ma sono molto piů penetranti delle a,
infatti, per bloccarle sono necessari circa 2m d’aria. Viaggiano ad una velocitŕ che
č circa il 90% di quella della luce (300000Km/s), e anche se ionizzano di meno
l’aria (possiedono carica negativa) sono molto piů pericolose delle radiazioni a.
>1 (dove n č
il numero dei neutroni e p quello dei protoni): il nucleo contiene troppi neutroni
rispetto ai protoni; diventa piů stabile se uno dei suoi neutroni decade a protone dando
luogo al decadimento b. Ciň significa che il numero
di massa rimane costante, ma il numero atomico Z aumenta per ogni decadimento b di un’unitŕ, poiché ogni neutrone
emettendo un elettrone (i cosiddetti raggi b) e un neutrino
(una particella di massa molto piů piccola di quella dell’elettrone) si
"trasforma" in un protone. Le cosiddette radiazioni b
sono sempre di natura corpuscolare ma sono molto piů penetranti delle a,
infatti, per bloccarle sono necessari circa 2m d’aria. Viaggiano ad una velocitŕ che
č circa il 90% di quella della luce (300000Km/s), e anche se ionizzano di meno
l’aria (possiedono carica negativa) sono molto piů pericolose delle radiazioni a.

Decadimento con emissione di raggi g. Queste radiazioni sono di natura elettromagnetica (e sono
quindi onde ricche di energia perché ad alta frequenza, elettricamente neutre e
praticamente prive di massa, a meno che non si consideri la natura corpuscolata dei "quanti" che viaggiano
con loro, ) e proprio per questo estremamente penetranti. Essendo tra tutte le onde
elettromagnetiche le piů energetiche (poiché hanno minima lunghezza d’onda e
massima frequenza) sono anche le piů pericolose perché, quando attraversano tessuti
organici sono carcerogene e mutagene. I raggi g vengono emessi
durante il decadimento a o b di
numerosi nuclidi radioattivi naturali o artificiali. In questo decadimento non si verifica
cambiamento del numero di massa o del numero atomico, ma si hanno variazioni di energia
all'interno del nucleo conseguenti all’assestamento dei nucleoni che, nel decadimento
a o b, non hanno ancora raggiunto il
minor contenuto energetico, trovandosi in uno stato eccitato; il ritorno allo stato di
energia minima avviene appunto con emissione di raggi g.
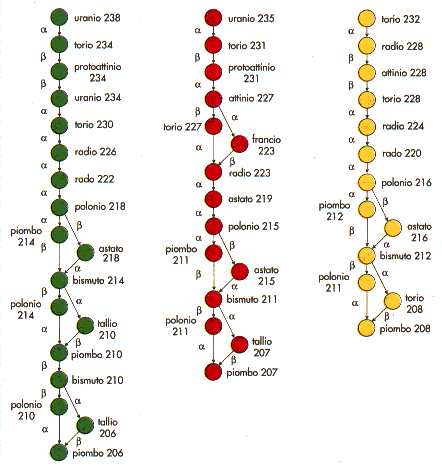 Decadimento
delle famiglie radioattive U 238,
Decadimento
delle famiglie radioattive U 238,
U 235 e Th 232. Come si puň vedere, in alcuni casi uno stesso nuclide puň disintegrarsi
in due modi diversi. Tutte e tre le famiglie conducono, comunque, a isotopi del piombo
stabili.